このページの目次
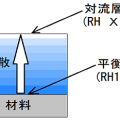
加熱乾燥の水の相変化
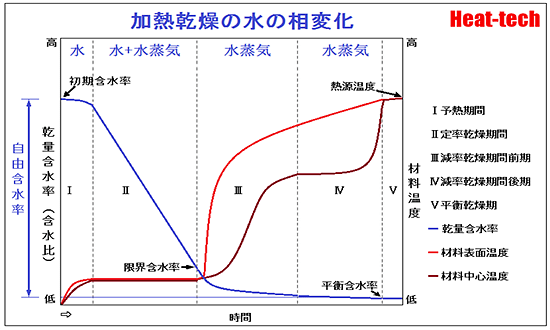
熱力学の区分では、乾燥工程は「開かれた系」です。
乾燥とは、「固体から液体を蒸発して分離すること」です。
熱、または、圧力を操作して、水を蒸発させて移動します。
熱の高低とは物質を構成する分子の運動の激しさ(大小)です。
圧力の大小とは、分子の数と分子運動の激しさです。

乾燥工程は、(窒素+酸素)=空気と水蒸気を対象とする、熱力学上の典型的な「3体問題」です。
「3体問題」とは「取り扱う物質が3個以上になると最早数学的な厳密解は得られない。」とされています。
厳密解が求められないことが定義されている以上、実用範囲の正確性で取り組む必要があります。
水は下記のような力で材料表面や内部に保有されています。
- 表面付着水→界面張力
- 毛管索状水→毛管吸引力
- 毛管懸吊水→界面張力
- オスモティック水→オスモティック吸引力
- 吸着水→吸着力
- 結合水→親和力
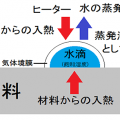
この力に対して熱や圧力を加えて液体を材料表面に移動して蒸発させます。
又は、材料内部で気化させて、材料表面に移動し放出します。
熱の伝達に使用する力は
- 熱伝導
水や蒸気の移動に使用する力は
- 拡散
蒸発に使用する力は
- 潜熱
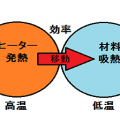
熱の移動は表面から内部へ
水分の移動は内部から表面へ
と逆方向に作用します。
乾燥工程で一番多いのは、熱を加える加熱乾燥です。
風を当てて表面を減圧して乾燥する風干しも一般的です。
冷却凍結した後、減圧して乾燥する真空乾燥も徐々に増えています。
*水と蒸気の相平衡
閉じた空間で水と水蒸気が共存した状態では、濃度平衡定数に達した時点で水の蒸発は止まります。
常温常圧(25℃・1atm)で水の中に含まれる蒸気は
水の生成自由エネルギー=-237.1KJ/mol
水蒸気の生成自由エネルギー=-228KJ/mol
H2O(liquid)→H2O(gas)+8.5kJ/mol at25℃・1atm
25℃の水の濃度平衡定数
Kc=[H2O(gas)]/[H2O(water)]=exp(-ΔG/RT)=exp(-8500/8.31×298)=0.03 at25℃・1atm
※ 8500=8.5kJ/mol
※ 298=K=273℃+25℃
∴水97% 水蒸気3% が平衡状態
60℃常圧(60℃・1atm)で水の中に含まれる蒸気は
水の生成自由エネルギー=-237.1KJ/mol
水蒸気の生成自由エネルギー=-228KJ/mol
60℃の水の定圧比熱 75.3J/K・mol
60℃の水蒸気の定圧比熱 33.6J/K・mol
ΔG(333)=8500+(-41.7)(333-298)-333(41.7)In333/298=8.5825kJ/mol
60℃の水の濃度平衡定数
Kc=[H2O(gas)]/[H2O(water)]=exp(-ΔG/RT)=exp(-858285/8.31×333)=0.045 at60℃・1atm
※ 8582.5=8.5825kJ/mol
※ 333=K=273℃+60℃
∴水95.5% 水蒸気4.5% が平衡状態
日常経験値と一致しますが、60℃に温度を上げれば、25℃を基準にすると1.5倍水蒸気になりやすくなります。
 非接触高温加熱・ハイテクヒーターのヒートテック 熱風ヒーター:ハロゲンヒーター:遠赤外ヒーター
非接触高温加熱・ハイテクヒーターのヒートテック 熱風ヒーター:ハロゲンヒーター:遠赤外ヒーター